⚠️RECORDATORIO: El mayor estudio de seguridad de la vacuna contra la COVID-19 jamás realizado, con 99 millones de personas, confirmó que las inyecciones NO SON SEGURAS PARA USO HUMANO:
➊ 610 % más de riesgo de miocarditis tras la inyección de la plataforma de ARNm.
➋ 378 % más de riesgo de encefalomielitis aguda diseminada (ADEM) tras la inyección de ARNm.
➌ 323 % más de riesgo de trombosis de senos venosos cerebrales (TSVC) tras la inyección de un vector viral.
➍ 249 % más de riesgo de síndrome de Guillain-Barré (SGB) tras la inyección de un vector viral.
Weil die Studie gerade wieder viel auf X geteilt wird: Wir haben die Erkenntnisse hier ausführlich dargestellt 👇🏻https://t.co/yUg6vJIRt7 https://t.co/VzWqAXCiYa
— ÄFI (@individ_impfen) March 18, 2025
❗❗El estudio observacional más grande del mundo confirma fuertes señales de seguridad para las vacunas contra la COVID-19❗❗
https://individuelle-impfentscheidung.de/aktuelles/detail/weltweit-groesste-beobachtungsstudie-bestaetigt-starke-sicherheitssignale-fuer-die-covid-19-impfstoffe.html
La lista de posibles efectos secundarios de las vacunas contra el coronavirus se ha vuelto cada vez más larga después de su lanzamiento, a pesar de las promesas de seguridad. Mientras tanto, dos de las cinco vacunas (ChAdOx1/Vaxzevria y Ad26.COV2-S/JCOVDEN) están restringidas a personas mayores de 60 años debido a eventos tromboembólicos más frecuentes, y otra vacuna (mRNA-1273/Spikevax) no se recomienda para personas menores de 30 años debido a un mayor riesgo de pericarditis y miocarditis. Un estudio recién publicado y a una escala sin precedentes ha confirmado una vez más las señales de seguridad descubiertas previamente.
En 2021, se lanzó el proyecto Global COVID Vaccine Safety (GCoVS) de la Global Vaccine Data Network™ (GVDN®) con financiación de los Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. para evaluar la seguridad de las vacunas contra la COVID-19. La urgencia del problema también fue evidente para la GVDN® porque una señal de seguridad solo pudo detectarse en grandes estudios de observación después de que millones de personas (incluidas las poblaciones vulnerables) ya habían sido vacunadas con las nuevas vacunas.
El objetivo del estudio GVDN® ahora publicado fue identificar señales de seguridad de 13 eventos adversos de interés especial (AESI) después de la vacunación contra la COVID-19. Para este propósito, se evaluaron datos sanitarios electrónicos de diez ubicaciones en ocho países diferentes, incluidos Argentina, Australia (Nueva Gales del Sur y Victoria), Canadá (Columbia Británica y Ontario), Dinamarca, Finlandia, Francia, Nueva Zelanda y Escocia. Los datos proceden, entre otros, de: de bases de datos de atención sanitaria, registros nacionales de vacunación y paneles de vacunación.
Cohorte de más de 99 millones de personas vacunadas
Finalmente, la cohorte incluyó más de 99 millones de personas vacunadas, la mayoría de las cuales tenían entre 20 y 39 años y entre 40 y 59, con un total de 183.559.462 dosis de BNT162b2/Corminaty, 36.178.442 de mRNA-1273/Spikevax y 23.093.399 de ChAdOx1/Vaxzevria. En Francia se administraron con diferencia el mayor número de vacunas (aproximadamente 121 millones).
Los resultados, que se clasificaron según enfermedades neurológicas, hematológicas y cardiovasculares, se presentan claramente en las Tablas 3 a 5 (ver a continuación) utilizando un sistema de semáforo (verde, amarillo, rojo). Los valores verdes deben entenderse como no estadísticamente significativos, los amarillos como estadísticamente significativos y los rojos como señal de seguridad estadísticamente significativa.
Quizás los resultados más interesantes: BNT162b2 y mRNA-1273 muestran consistentemente una fuerte señal de seguridad para la miocarditis después de la primera, segunda y tercera dosis. El ARNm-1273 también muestra una señal de seguridad para la pericarditis después de la primera y tercera vacunación, ChAdOx1 después de la segunda vacunación.
Aunque hubo algunos resultados estadísticamente significativos para las enfermedades hematológicas después de la primera vacunación, solo se observó una señal de seguridad para la trombosis de la vena del seno cerebral (TSVC) después de la primera dosis de ChAdOx1. Lo mismo se aplica a las enfermedades neurológicas: aquí, los resultados para ChAdOx1 indican un riesgo para el desarrollo del síndrome de Guillain-Barré (SGB), y para mRNA-1273 para el desarrollo de encefalomielitis diseminada aguda (ADEM), ambos después de la primera vacunación.


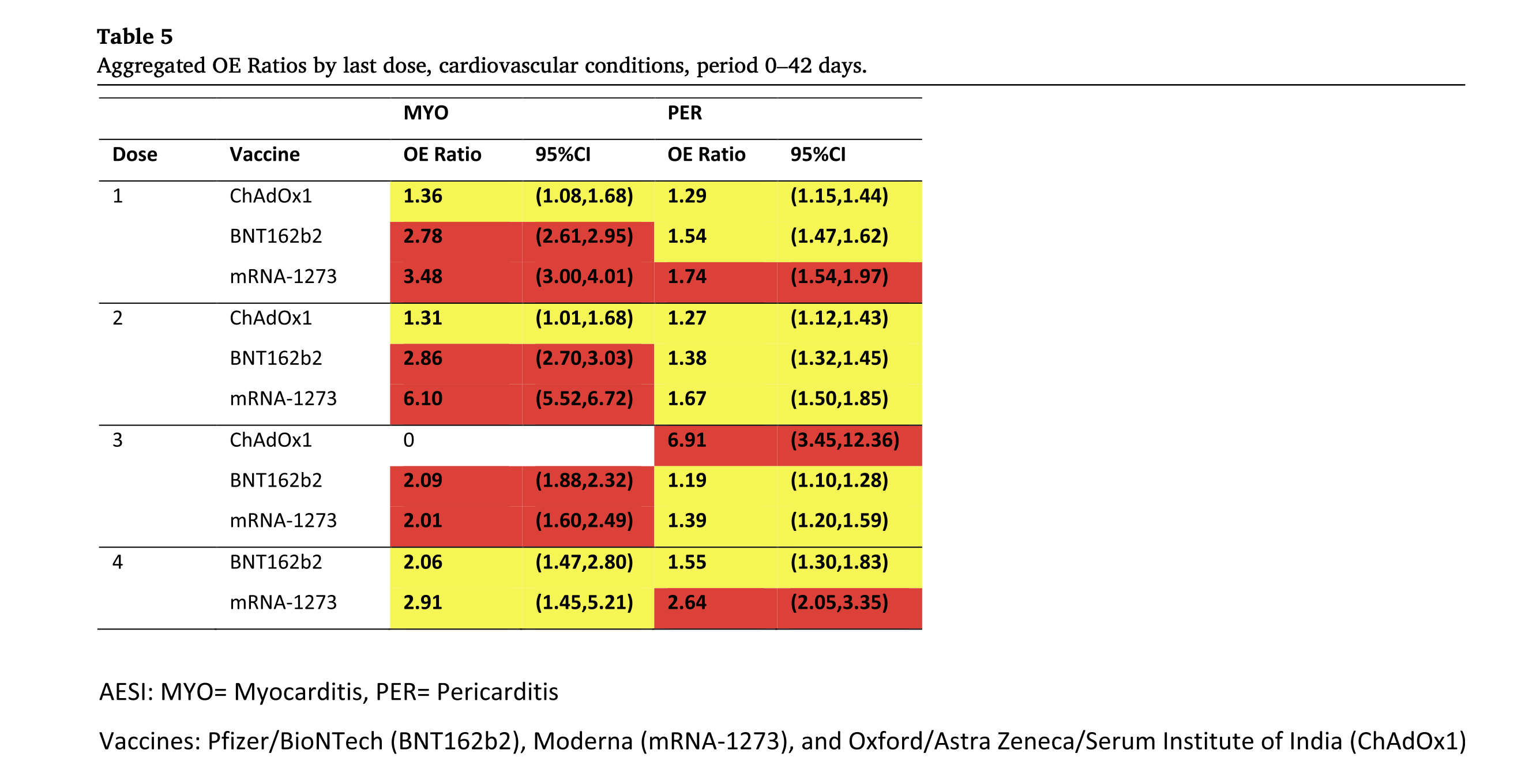
Figura: Tablas 3 a 5 del estudio de Faksova et al. (2024). Las vacunas BNT162b2/Corminaty, mRNA-1273/Spikevax y ChAdOx1/Vaxzevria se clasifican según el número de dosis administradas. En la Tabla 3 se muestran los resultados para el riesgo de enfermedades neurológicas según el esquema del semáforo mencionado anteriormente, la Tabla 4 para las enfermedades hematológicas y la Tabla 5 para las enfermedades cardiovasculares. Umbrales para evidencia estadística de posibles señales – Rojo: LBCI* >1,5, señal de seguridad estadísticamente significativa; Amarillo: LBCI* >1 y <1,5, estadísticamente significativo; Verde: LBCI* <1,0, no estadísticamente significativo; *LBCI: Límite inferior del intervalo de confianza.
Cabe señalar que BNT162b2 se administró con mucha más frecuencia que las otras dos vacunas. Además, existe cierta heterogeneidad en la recopilación de datos, la calidad y los estándares de presentación de informes entre los países, lo que en última instancia significa que no se pueden descartar distorsiones en la comparabilidad.
Por ejemplo, las campañas de vacunación en distintos países se diseñaron de manera diferente en términos de priorización de los receptores de la vacuna, los tipos de vacunas y los regímenes de dosificación. Un estudio de Nature publicado en febrero de 2024 encontró un riesgo 66% menor de carditis cuando el intervalo entre el primer y el segundo BNT162b2 se incrementó de 21 a 27 días a ≥ 56 en adolescentes varones (Fan et al., 2024). Las diferentes regulaciones respecto al intervalo entre las series de vacunación y las diferencias específicas de la población (condiciones de salud existentes, genética, comportamiento) son sólo dos de los muchos ejemplos de factores de confusión en un estudio observacional. Sin embargo, como la mayor parte de los datos de este estudio proceden de Francia, este último punto puede tener menos importancia.
Reconsiderar la recomendación de vacunación contra STIKO
En conclusión, el estudio de Faksova et al. (2024) no necesariamente aportó nuevos conocimientos, pero contribuyó a la validez de estudios anteriores, en su mayoría de ámbito nacional.
También es interesante reflexionar sobre la recomendación de vacunación de STIKO en este contexto: STIKO no recomienda mRNA-1273/Spikevax para personas menores de 30 años debido a un mayor riesgo de desarrollar miocarditis o pericarditis. Sin embargo, lo mismo debería aplicarse también a BNT162b2/Corminaty debido a un mayor riesgo de desarrollar miocarditis. Especialmente porque el riesgo en este estudio fue mayor después de la tercera dosis de BNT162b2/Corminaty que con mRNA-1273/Spikevax.
Como se pide en el documento de posición de ÄFI “Por un replanteamiento de la política de vacunación”, debería realizarse una revisión científica exhaustiva del uso masivo de las nuevas vacunas contra el coronavirus. Esto también incluye garantizar que esta nueva publicación se dé a conocer a los círculos profesionales pertinentes.

No hay comentarios:
Publicar un comentario