Los chips de órganos humanos permiten una rápida reutilización de medicamentos para COVID-19
La emulación de las vías respiratorias pulmonares humanas in vitro identificó efectos útiles del fármaco antipalúdico amodiaquina, ahora en ensayos clínicos
La colaboración liderada por AWyss Institute que abarca cuatro laboratorios de investigación y cientos de millas ha utilizado la tecnología de órgano en un chip (Organ Chip) del instituto para identificar el medicamento antipalúdico amodiaquina como un potente inhibidor de la infección con SARS-CoV-2, el virus que causa el COVID-19.
El ecosistema de prueba de drogas basado en Organ Chip establecido por la colaboración agiliza en gran medida el proceso de evaluación de la seguridad y la eficacia de los medicamentos existentes para nuevas aplicaciones médicas, y proporciona una prueba de concepto para el uso de Organ Chips para reutilizar rápidamente los medicamentos existentes para nuevas aplicaciones médicas, incluidas futuras pandemias. La investigación se informa en Nature Biomedical Engineering.
Si bien muchos grupos de todo el mundo han estado probando la eficacia de medicamentos existentes contra el COVID-19 utilizando células cultivadas, es bien sabido que las células cultivadas en un plato no se comportan como las células en un cuerpo humano vivo, y muchos medicamentos que parecen efectivos en los estudios de laboratorio no funcionan en los pacientes. El equipo de Wyss examinó ocho medicamentos existentes, incluidas la hidroxicloroquina y la cloroquina, que ellos y otros habían descubierto que eran activos contra el SARS-CoV-2 en ensayos de cultivos celulares convencionales.
Cuando se probaron en su Lung Airway Chip microfluídico más sofisticado, que había sido infectado con un virus SARS-CoV-2 pseudotipado, descubrieron que la mayoría de estos medicamentos, incluidas la hidroxicloroquina y la cloroquina, no eran efectivos. Sin embargo, otro fármaco antipalúdico, la amodiaquina, fue muy eficaz para prevenir la entrada del virus. Luego, estos resultados se validaron en células cultivadas y en un modelo animal pequeño de COVID-19 utilizando el virus infeccioso SARS-CoV-2. La amodiaquina ahora se encuentra en ensayos clínicos para COVID-19 en múltiples sitios en África, donde este medicamento es económico y está ampliamente disponible.
“La velocidad con la que este equipo se reunió, giró hacia COVID-19 y produjo resultados clínicamente significativos es asombrosa”, dijo el autor principal y director fundador del Instituto Wyss, Don Ingber. “Comenzamos a probar estos compuestos en febrero de 2020, teníamos datos en marzo y publicamos una versión preliminar en abril. Gracias a la apertura y colaboración que la pandemia ha suscitado dentro de la comunidad científica, nuestro fármaco principal ahora se está probando en humanos. Es un poderoso testimonio de la capacidad de Organ Chips para acelerar las pruebas preclínicas”.
De enfermedad misteriosa a compuesto de plomo en meses
En los primeros meses de la pandemia de COVID-19, cuando se sabía poco sobre el nuevo virus SARS-CoV-2, se realizaron esfuerzos en todo el mundo para identificar los medicamentos existentes que podrían reutilizarse para tratar a los pacientes que se enfermaban. Si bien los primeros datos realizados en células cultivadas en placas de laboratorio parecían sugerir que los medicamentos antipalúdicos cloroquina e hidroxicloroquina podrían tratar la enfermedad, estudios posteriores demostraron que no son activos contra el SARS-CoV-2 en animales o pacientes, y la búsqueda de un La terapéutica oral efectiva que puede tratar y prevenir el COVID-19 continúa.
Afortunadamente, el Instituto Wyss tenía una solución preparada para ese problema. En un movimiento que hoy parece profético, hace más de tres años la Agencia de Proyectos de Investigación Avanzada de Defensa (DARPA) y los Institutos Nacionales de Salud (NIH) otorgaron fondos al equipo de Ingber para explorar si su tecnología de cultivo de microfluidos Organ Chip humano, que imita fielmente la función de órganos humanos in vitro, podría usarse para enfrentar posibles desafíos de amenazas biológicas, incluidos los virus respiratorios pandémicos.
Dos años después de iniciado el proyecto, el equipo estaba haciendo un progreso constante utilizando su chip Airway de pulmón para estudiar medicamentos que podrían reutilizarse para tratar infecciones por el virus de la influenza. Luego, en enero de 2020, los primeros autores Longlong Si y Haiqing Bai se enteraron de casos de lo que se llamaba una nueva neumonía viral en China.
“Eso llamó mucho la atención de los científicos, porque cualquier virus nuevo podría convertirse en una amenaza global dada la facilidad con la que las infecciones se propagan en la era actual de viajes internacionales generalizados. Seguimos de cerca las actualizaciones porque pensamos que nuestro modelo Airway Chip podría proporcionar una herramienta importante para estudiar este virus”, dijo Si, becario de desarrollo de tecnología de Wyss y coautor principal. Una vez que quedó claro que las personas se estaban enfermando debido al misterioso COVID-19 y no a la neumonía, el equipo cambió rápidamente su enfoque al nuevo virus SARS-CoV-2.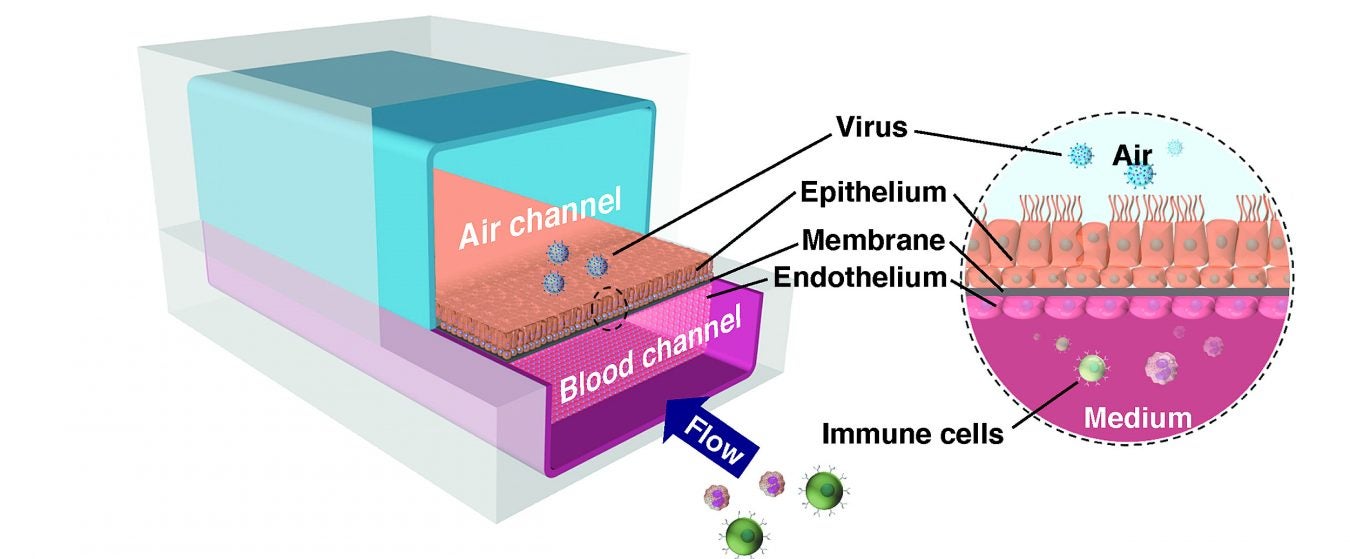
El Airway Chip humano recrea la interfaz de las vías respiratorias y los vasos sanguíneos del pulmón humano, lo que permite a los investigadores estudiar cómo diferentes fármacos y patógenos, como los virus, afectan la función pulmonar. Crédito: Instituto Wyss de la Universidad de Harvard
El Airway Chip humano que el equipo de Wyss desarrolló para estos estudios es un dispositivo de microfluidos del tamaño de una memoria USB que contiene dos canales paralelos separados por una membrana porosa. Las células de las vías respiratorias de los pulmones humanos se cultivan en un canal que se perfunde con aire, mientras que las células de los vasos sanguíneos humanos se cultivan en el otro canal, que se perfunde con un medio de cultivo líquido para imitar el flujo sanguíneo. Las células cultivadas en este dispositivo se diferencian naturalmente en múltiples tipos de células específicas de las vías respiratorias en proporciones similares a las de las vías respiratorias humanas, y desarrollan rasgos observados en los pulmones vivos, como los cilios y la capacidad de producir y mover moco. Las células Airway Chip también tienen niveles más altos de proteína receptora de la enzima convertidora de angiotensina 2 (ACE2), que desempeña un papel central en la fisiología pulmonar y es utilizada por el SARS-CoV-2 para infectar las células.
“Nuestro mayor desafío al cambiar nuestro enfoque al SARS-CoV-2 fue que no tenemos instalaciones de laboratorio con la infraestructura necesaria para estudiar patógenos peligrosos de manera segura. Para solucionar ese problema, diseñamos un pseudovirus SARS-CoV-2 que expresa la proteína de punta del SARS-CoV-2, de modo que pudiéramos identificar medicamentos que interfieren con la capacidad de la proteína de punta para unirse a los receptores ACE2 de las células pulmonares humanas”. dijo Bai, quien es becario postdoctoral en el Instituto Wyss y coautor principal. “Un objetivo secundario era demostrar que este tipo de estudios podrían ser realizados por otros investigadores de Organ Chip que también tienen esta tecnología, pero carecen de acceso a las instalaciones de laboratorio necesarias para estudiar virus altamente infecciosos”.
Armados con el pseudovirus que les permitió estudiar la infección por SARS-CoV-2, el equipo perfundió primero el canal de vasos sanguíneos de los Airway Chips con varios medicamentos aprobados, incluidos amodiaquina, toremifeno, clomifeno, cloroquina, hidroxicloroquina, arbidol, verapamilo y amiodarona. todos los cuales han exhibido actividad contra otros virus relacionados en estudios previos. Sin embargo, a diferencia de los estudios de cultivos estáticos, pudieron perfundir el fármaco a través de los canales del chip usando una dosis clínicamente relevante para imitar cómo se distribuiría el fármaco a los tejidos de nuestro cuerpo. Después de 24 horas, introdujeron el pseudovirus SARS-CoV-2 en el canal de aire de los Airway Chips para imitar la infección por virus en el aire, como la tos o el estornudo.
Solo tres de estos medicamentos (amodiaquina, toremifeno y clomifeno) impidieron significativamente la entrada viral sin producir daño celular en los Airway Chips. El fármaco más potente, la amodiaquina, redujo la infección en un 60 por ciento. El equipo también realizó mediciones de espectrometría con la ayuda del grupo de Steve Gygi en la Escuela de Medicina de Harvard para evaluar cómo los medicamentos impactaron en las células de las vías respiratorias. Estos estudios revelaron que la amodiaquina produjo cambios proteicos distintos y más amplios que los otros medicamentos antipalúdicos.
Los investigadores tenían un candidato a fármaco líder.
Todas las manos en el mazo
A pesar de la promesa de la amodiaquina, el equipo aún necesitaba demostrar que funcionaba contra el verdadero virus infeccioso SARS-CoV-2. Con la ayuda de una nueva subvención centrada en COVID-19 de DARPA, Ingber se asoció con Matthew Frieman en la Facultad de Medicina de la Universidad de Maryland y Benjamin tenOever en la Facultad de Medicina Icahn en Mount Sinai, quienes ya tenían laboratorios de bioseguridad establecidos. para estudiar patógenos infecciosos.
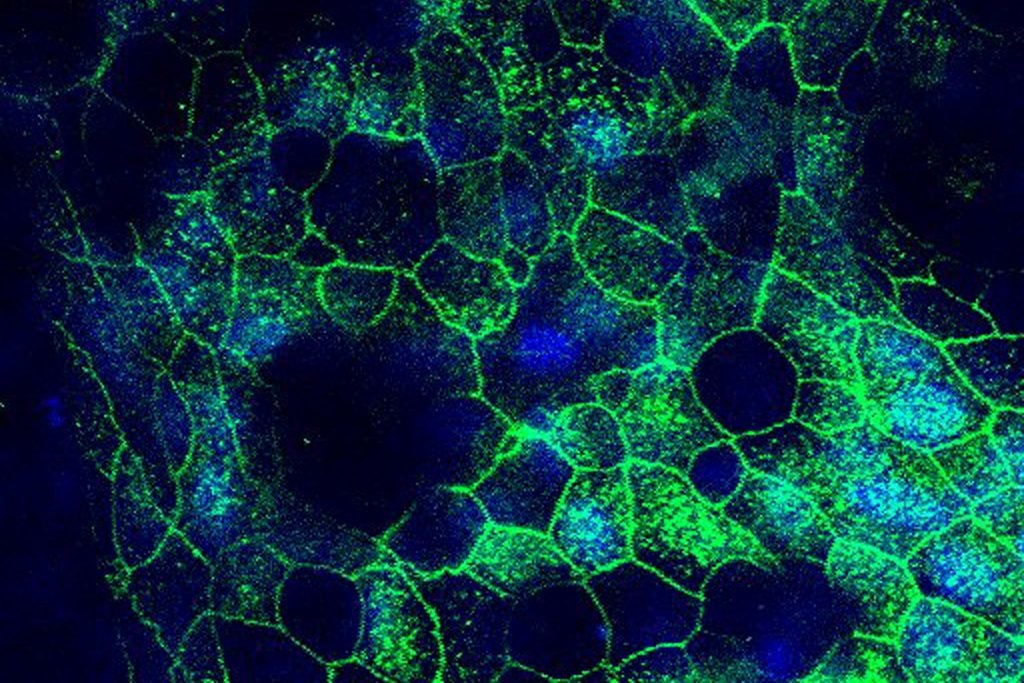
Esta colaboración creó un ecosistema de descubrimiento de fármacos que combina la capacidad de emulación humana de los chips de órganos del Instituto Wyss con la experiencia de Frieman y tenOever en las interacciones entre los virus y sus células anfitrionas. El laboratorio de Frieman probó la amodiaquina y su metabolito activo, la desetilamodiaquina, contra el SARS-CoV-2 nativo a través de ensayos de alto rendimiento en células in vitro y confirmó que el fármaco inhibía la infección viral.
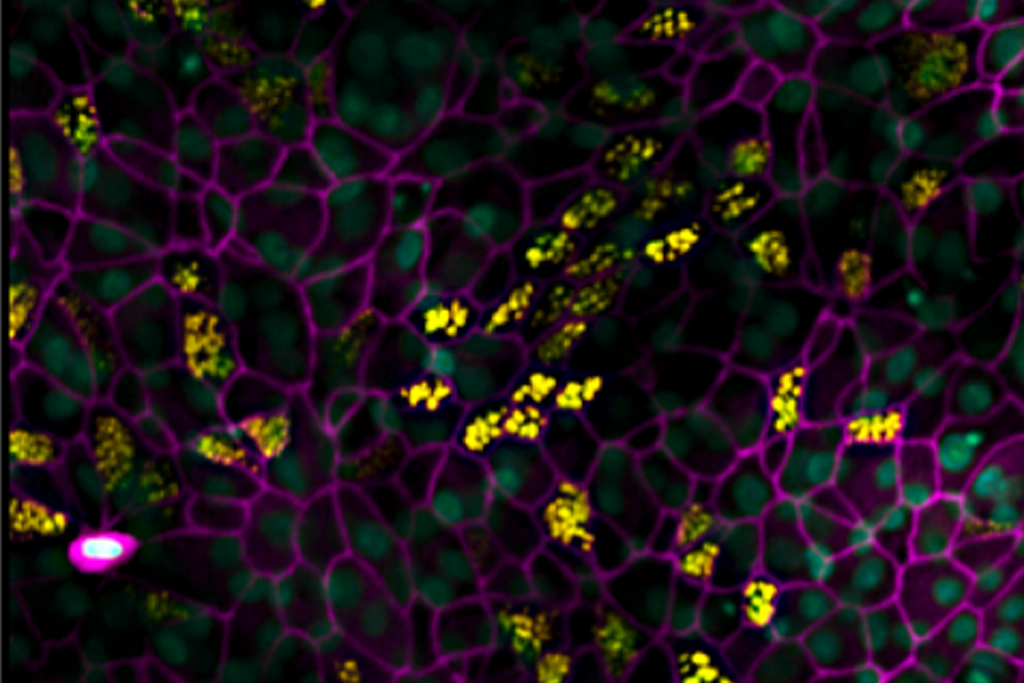
Paralelamente, el laboratorio tenOever probó la amodiaquina y la hidroxicloroquina contra el SARS-CoV-2 nativo en una comparación directa en un modelo de COVID-19 de animales pequeños, y vio que el tratamiento profiláctico con amodiaquina resultó en una reducción de alrededor del 70 por ciento en la carga viral tras la exposición, mientras que la hidroxicloroquina fue ineficaz. También vieron que la amodiaquina prevenía la transmisión del virus de animales enfermos a sanos más del 90 por ciento de las veces, y que también era eficaz para reducir la carga viral cuando se administraba después de la introducción del virus. Por lo tanto, sus resultados sugieren que la amodiaquina podría funcionar tanto en el modo de tratamiento como en el de prevención.
"Ver cómo la amodiaquina inhibió maravillosamente la infección en el Airway Chip fue extremadamente emocionante", dijo Frieman. “Y el hecho de que parezca funcionar tanto antes como después de la exposición al SARS-CoV-2 significa que podría ser potencialmente efectivo en una amplia variedad de entornos”.
“Esta colaboración nos ha permitido hacer cosas que nunca hubiéramos tenido los recursos para hacer de otra manera, incluida la instalación reciente de Organ Chips en nuestro propio laboratorio para que ahora podamos usarlos para estudiar las interacciones entre los virus infecciosos y sus anfitriones. Si bien estamos orgullosos de lo que hemos logrado hasta ahora para COVID-19, también esperamos estudiar dinámicas adicionales de virus-huésped utilizando los chips de órgano con la esperanza de que podamos prevenir o abordar futuras pandemias. ”, dijo tenOever, quien es profesor de microbiología.
Una preimpresión de los resultados de la amodiaquina se publicó en línea el 15 de abril de 2020, lo que generó entusiasmo en la comunidad científica. Eventualmente llamó la atención de Medicines for Malaria Venture, una asociación líder en el desarrollo de productos en la investigación de medicamentos antipalúdicos. Estos resultados, junto con los estudios de varios otros grupos, contribuyeron a la inclusión de la amodiaquina en un ensayo clínico en colaboración con la Universidad de Witwatersrand en Sudáfrica y Shin Poong Pharmaceutical en Corea del Sur el otoño pasado. Unos meses más tarde, la Iniciativa de Medicamentos para Enfermedades Olvidadas (DNDi) agregó amodiaquina al ensayo clínico ANTICOV para COVID-19, que abarca 19 sitios en más de 13 países diferentes en África. La amodiaquina es oral, extremadamente económica y ampliamente disponible en África. Si se demuestra su eficacia en estos ensayos clínicos, podría proporcionar un arma muy necesaria contra el COVID-19 en países de bajos recursos donde el acceso a vacunas y nuevas terapias costosas es limitado.
Preparándonos para la próxima pandemia
Si bien la identificación de la amodiaquina es una gran ayuda en la lucha contra el COVID-19, el equipo ya tiene la vista puesta en futuras pandemias. Además del SARS-CoV-2, su publicación reciente detalla su éxito en la búsqueda de medicamentos que podrían proteger o tratar varias cepas del virus de la influenza.
"Gracias a nuestra experiencia en el uso de esta línea de desarrollo de fármacos para validar la amodiaquina para el COVID-19, ahora estamos aplicando lo que aprendimos a la influenza y otros patógenos que causan pandemias", dijo el coautor Ken Carlson, científico principal del personal sénior que ayuda a dirigir el Equipo del Proyecto Terapéutico de Coronavirus en el Instituto Wyss. “Este proceso nos ha dado la confianza de que los Organ Chips predicen lo que vemos en modelos vivos más complejos de infecciones virales y ayudó a aprovechar el caldero creativo del Instituto Wyss para consolidar y fortalecer nuestro motor de descubrimiento terapéutico”.
Además de la influenza, el equipo ahora está explorando medicamentos que podrían usarse contra las nuevas cepas mutantes de SARS-CoV-2, para suprimir la peligrosa "tormenta de citoquinas" que conduce a muchas hospitalizaciones y para aliviar los síntomas de COVID-19. los de larga distancia”.
“La pandemia realmente ha solidificado el programa de desarrollo de Terapéutica Bioinspirada del Instituto Wyss, y la vinculación con los laboratorios Frieman y tenOever ha creado una tubería de descubrimiento y desarrollo de fármacos que acelera drásticamente todo el proceso, guiando rápidamente los medicamentos contra el COVID-19 a través del desarrollo preclínico hasta el punto donde se pueden probar en humanos. Con la tecnología Organ Chip en la mano, ahora estamos en una posición más sólida para enfrentar futuras pandemias”, dijo Ingber, quien también es profesor Judah Folkman de Biología Vascular en la Escuela de Medicina de Harvard y el Hospital Infantil de Boston, y profesor de Bioingeniería en la Universidad John de Harvard. A. Escuela Paulson de Ingeniería y Ciencias Aplicadas.
Otros autores del artículo incluyen a Melissa Rodas, Wuji Cao, Crystal Oh, Mercy Soong,
Atiq Nurani, Seong Min Kim, Danni Zhu, Girija Goyal, Rani Powers y Roberto Plebiani del Instituto Wyss; los ex miembros del Instituto Wyss Rachelle Prantil-Baun, Kambez Benam y Sarah Gilpin; Amanda Jiang del Boston Children's Hospital y la Harvard Medical School; Rasmus Moller, Daisy Hoagland, Kohei Oishi, Shu Horiuchi, Skyler Uhl, Daniel Blanco-Melo, Tristan Jordan, Benjamin Nilsson-Payant, Ilona Golynker y Justin Frere de la Escuela de Medicina Icahn en Mount Sinai; James Logue, Robert Haupt, Marisa McGrath y Stuart Weston de la Facultad de Medicina de la Universidad de Maryland; Tian Zhang y Steve Gygi de la Escuela de Medicina de Harvard.
Esta investigación fue apoyada por NIH (NCATS 1-UG3-HL-141797-01 y NCATS 1-UH3-HL-141797-01), DARPA (W911NF-12-2-0036 y W911NF-16-C-0050), la Fundación Bill y Melinda Gates, la Fundación Marc Haas y el Instituto Wyss de Ingeniería de Inspiración Biológica de la Universidad de Harvard.

No hay comentarios:
Publicar un comentario